 |
|
 04.09.2008, 18:04
04.09.2008, 18:04
|
#61
|
|
Живу я тут
Регистрация: 28.06.2003
Адрес: Киев
Сообщений: 757
Поблагодарил(а) : 831
Поблагодарили 833 раз(а) в 397 сообщениях
|
Відповідь: Ответ: Відповідь: Хелат железа. Химики, обьясните. ===www.aquaforum.ua===
Цитата:
Сообщение от Кокан

Вот только ЭДТА не 4-, а 2/4- (4 кислорода и 2 азота) выглядит примерно так - .
|
Согласен. Но в таком случае надо бы говорить не о валентности ЭДТА, а о его дентатности, равной 6.
Цитата:
Сообщение от Кокан

У FeH2(Edta) два координационных места занято ещё одним лигандом - водородом и это вещество не расстворимо. А вот в присутствии других орг. кислот нерастворимого осадка не получается, не потому ли это, что эти два места не дают занять молекулы этих кислот - тоже вданном случае лиганды одного комплекса - полилигандного?
|
Я встречал информацию, что у подобных комплексов протоны H+ присоединяются к карбоксильным группам, понижая дентатность ЭДТА и устойчивость комплекса, а освободившиеся координационные места занимают молекулы воды. Но это, в сущности, не повлияет на ход дальнейших рассуждений о пользе органических кислот.
Ну да ладно. Если смесь работает лучше, значит есть на то причина, пусть и неочевидная.
|

|

|
|
Пользователь, который поблагодарил Володя Череп за данный пост:
|
|
 04.09.2008, 19:15
04.09.2008, 19:15
|
#62
|
|
Любитель отечественной флоры и фауны
Регистрация: 03.11.2003
Адрес: Киев
Сообщений: 5,563
Поблагодарил(а) : 4,179
Поблагодарили 3,075 раз(а) в 1,438 сообщениях
|
Ответ: Відповідь: Ответ: Відповідь: Хелат железа. Химики, обьясните. ===www.aquaforum.ua===
Цитата:
Сообщение от Володя Череп

а освободившиеся координационные места занимают молекулы воды
|
Это даже совсем не обязательно. Наиболее характерные координационные числа для железа 2+ и 3+ - это: 4, 6 и 5,7... Но конкретно чего там может получится в этом нерастворимом комплексе я не знаю. Это просто так - повыпендриваццо.
__________________
Ψ http://florastim.com.ua/
|

|

|
 13.09.2008, 18:29
13.09.2008, 18:29
|
#63
|
|
Живу я тут
Регистрация: 31.01.2007
Адрес: Киев
Сообщений: 2,744
Поблагодарил(а) : 535
Поблагодарили 6,235 раз(а) в 1,351 сообщениях
|
Ответ: Хелат железа. Химики, обьясните. ===www.aquaforum.ua===
Цитата:
Сообщение от Виктор У

Разводил так: порошка насыпал 4мл, затем разбавил в 250мл, после этого 5мл в акву(300л). Тетровский тест через час показывал примерно 0.5мг/л, на следующий день дозу увеличил в два раза тест показывал 0.1мг/л, примерно часа через 4 железа было в два раза меньше (вот и хваленые супер хелаты). Да, и когда выливается он зрелище жуткое. Если не открывал отнеси назад, возьми у меня попробуй.
|
Я уже вскрыл... раствор у меня с другими цифрами ( очень похожими  )
8.3 г в 100 мг, и из этого раствора 1мл на 10 литров аквариумной воды добавляем железо.
Вот я добавил 2 мл на 20 литров (сливал воду с аквариума - решил поэкспериментировать) - смотрите что получилось.
А то, что получилось - мне очень не нравится!

Мой пост № 10, как и предложение в нем- прошу считать ошибочным...
не подходит Ferrilen 4.8 для использования в аквариуме!
__________________
[URL="http://dramader.blogspot.com/"]Посетите мой блог[/URL]
Последний раз редактировалось BЛАДИМИP; 26.09.2008 в 15:24..
|

|

|
|
Пользователь, который поблагодарил BЛАДИМИP за данный пост:
|
|
 13.09.2008, 21:49
13.09.2008, 21:49
|
#64
|
|
Живу я тут
Регистрация: 20.02.2008
Адрес: одесса
Сообщений: 320
Поблагодарил(а) : 106
Поблагодарили 36 раз(а) в 30 сообщениях
|
Ответ: Хелат железа. Химики, обьясните. ===www.aquaforum.ua===
Цитата:
Сообщение от Bactrian

А то, что получилось - мне очень не нравится!
не подходит Ferrilen 4.8 для использования в аквариуме!
|
А что....?..вполне приличный натюрморт..!  .  
Можно натурально заборы красить...Кстати я из этой благородной химии
воще ничего в Одессе найти не могу...
|

|

|
 13.09.2008, 23:47
13.09.2008, 23:47
|
#65
|
|
Живу я тут
Регистрация: 31.01.2007
Адрес: Киев
Сообщений: 2,744
Поблагодарил(а) : 535
Поблагодарили 6,235 раз(а) в 1,351 сообщениях
|
Ответ: Хелат железа. Химики, обьясните. ===www.aquaforum.ua===
Цитата:
Сообщение от Serpentarius

Bactrian, красящие растворы этой фирмы (в частности, Диссолвин 11% железа) благополучно обесцвечивает соляной кислотой Рома Тараненко - известный травник. При этом свойства удобрения не теряются
|
А в чем прикол, собственно?
Повысить кислотность и развалить хелатный комплакс железа!!!!????!!!
А этот "Феррилен 4.8", кстати, достаточно устойчив именно при низких рН, -это его основное достоинство, и я именно по этому его и покупал.
Чего-то я не понимаю логики - взять хелат железа (типа, чтобы устойчивый был и железо держал в растворенном состоянии в аквариуме -да?) залить его солянкой - типа разрушить хелат - и что мы в результате в аквариум льём?
Нехелатированное железо?
Или я чего-то не понимаю?
__________________
[URL="http://dramader.blogspot.com/"]Посетите мой блог[/URL]
Последний раз редактировалось BЛАДИМИP; 14.09.2008 в 11:14..
|

|

|
|
Пользователь, который поблагодарил BЛАДИМИP за данный пост:
|
|
| Реклама помогает развиваться |
|
|
 14.09.2008, 00:47
14.09.2008, 00:47
|
#66
|
|
Живу я тут
Регистрация: 09.10.2005
Адрес: Киев
Сообщений: 10,139
Поблагодарил(а) : 11,373
Поблагодарили 9,058 раз(а) в 4,069 сообщениях
|
Відповідь: Хелат железа. Химики, обьясните. ===www.aquaforum.ua===
Добавление кислоты не повышает, а понижает рН  А вот почему подкисление приводит к обесцвечиванию и не разрушается ли комплекс - не знаю. Может Володя Череп подскажет. А вообще все это алхимия. Если железо в комплексе - оно явно реакционно не доступно. Как распадается комплекс в аквариуме (линейно, логарифмически, моментально) - никто особо не мерял. Как быстро 2+ переходит в 3+ - тоже.
Последний раз редактировалось Mykhaylo; 14.09.2008 в 00:58..
|

|

|
 14.09.2008, 01:32
14.09.2008, 01:32
|
#67
|
|
Любитель отечественной флоры и фауны
Регистрация: 03.11.2003
Адрес: Киев
Сообщений: 5,563
Поблагодарил(а) : 4,179
Поблагодарили 3,075 раз(а) в 1,438 сообщениях
|
Ответ: Відповідь: Хелат железа. Химики, обьясните. ===www.aquaforum.ua===
Mykhaylo, Ты с кем сейчас разговаривал?
Добавлено через 18 минут
Главное ьлить в аквариум залезо шоб зелёное было. Это показатель 2+ . все , что не красное, то 2+. А вот если - 3+ на вас нападут водоросли, которые не попустят вас до конца..... А 3+ это красное. Бойтесь красного. ПРИМУ БЕЗ ФИЛЬТРА КУРИТЬ - ЗАПАДЛО!!!!!!
__________________
Ψ http://florastim.com.ua/
Последний раз редактировалось Кокан; 14.09.2008 в 01:51..
Причина: Добавлено сообщение
|

|

|
 14.09.2008, 11:23
14.09.2008, 11:23
|
#68
|
|
Живу я тут
Регистрация: 31.01.2007
Адрес: Киев
Сообщений: 2,744
Поблагодарил(а) : 535
Поблагодарили 6,235 раз(а) в 1,351 сообщениях
|
Ответ: Відповідь: Хелат железа. Химики, обьясните. ===www.aquaforum.ua===
Цитата:
Сообщение от Mykhaylo

Если железо в комплексе - оно явно реакционно не доступно. Как распадается комплекс в аквариуме (линейно, логарифмически, моментально) - никто особо не мерял. Как быстро 2+ переходит в 3+ - тоже.
|
Так там же органическая молекула EDDHSA, составляющая 94% комплекса
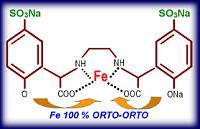
- вот она при добавлении солянки и разрушается, ибо устойчива до рН=3. ИМХО.
И остается катион железа, который по быстренькому, находит с чем связаться в растворе... и связывается ... или не находит... и тогда плавает как г...но в ополонке, но и его при этом ничто не защищает.
И вот такую "бурду" лить в аквариум?
Наверное это правильно, я ж не спорю...
Только мне как-то больше цитрат железа греет душу. 
Просто, дешево и эффективно...
__________________
[URL="http://dramader.blogspot.com/"]Посетите мой блог[/URL]
|

|

|
 14.09.2008, 11:24
14.09.2008, 11:24
|
#69
|
|
Живу я тут
Регистрация: 09.10.2005
Адрес: Киев
Сообщений: 10,139
Поблагодарил(а) : 11,373
Поблагодарили 9,058 раз(а) в 4,069 сообщениях
|
Відповідь: Хелат железа. Химики, обьясните. ===www.aquaforum.ua===
2 Кокан
Зеленое и желтое железо - это для сульфата без комплексона.
В составе комплекса с ЭДТА железо что 2+, что 3+ - желтое. 
А курить вообще вредно, неважно что. 
2 Bactrian
Я не настаиваю что обесцвечивать кислотой - правильно, я не знаю что при этом происходит. Может туда краситель добавляют для пущего эффекта, как в тотему тутти-фрутти.
Судя по графикам до рН 3 не разрушается. Как по мне, то если хочется железа 2+, но нужно делать капельную подачу (или хотя бы ежедневное внесение) и не заморачиваться с устойчивостью комплекса и т.п.
|

|

|
 14.09.2008, 12:01
14.09.2008, 12:01
|
#70
|
|
Живу я тут
Регистрация: 31.01.2007
Адрес: Киев
Сообщений: 2,744
Поблагодарил(а) : 535
Поблагодарили 6,235 раз(а) в 1,351 сообщениях
|
Ответ: Відповідь: Хелат железа. Химики, обьясните. ===www.aquaforum.ua===
Цитата:
Сообщение от Mykhaylo

Я не настаиваю что обесцвечивать кислотой - правильно, я не знаю что при этом происходит. Может туда краситель добавляют для пущего эффекта, как в тотему тутти-фрутти.
Судя по графикам до рН 3 не разрушается. Как по мне, то если хочется железа 2+, но нужно делать капельную подачу (или хотя бы ежедневное внесение) и не заморачиваться с устойчивостью комплекса и т.п.
|
Куплю кислоты попробую... что там происходит.
Но, вот с чем согласен полностью - так это с частым внесением железа в аквариум... я вношу через день.
__________________
[URL="http://dramader.blogspot.com/"]Посетите мой блог[/URL]
|

|

|
 14.09.2008, 20:05
14.09.2008, 20:05
|
#71
|
|
Живу я тут
Регистрация: 28.06.2003
Адрес: Киев
Сообщений: 757
Поблагодарил(а) : 831
Поблагодарили 833 раз(а) в 397 сообщениях
|
Відповідь: Ответ: Відповідь: Хелат железа. Химики, обьясните. ===www.aquaforum.ua===
Цитата:
Сообщение от Bactrian

Чего-то я не понимаю логики - взять хелат железа ... залить его солянкой - типа разрушить хелат - и что мы в результате в аквариум льём? Нехелатированное железо?
|
Залили солянкой - разрушили хелат, налили в аквариум - восстановили хелат.
Цитата:
Сообщение от Mykhaylo

А вот почему подкисление приводит к обесцвечиванию и не разрушается ли комплекс - не знаю. Может Володя Череп подскажет.
|
Происходит то же, что и с ЭДТА - лиганд протонируется и исходный комплекс разрушается (точнее говоря, равновесие смещается в сторону уменьшения концентрации исходного комплекса). Приводит ли это к обесцвечиванию, или нет - не могу сказать.
Цитата:
Сообщение от Mykhaylo

Если железо в комплексе - оно явно реакционно не доступно.
|
В комплексе находится большая часть железа. Меньшая часть железа находится в виде свободных катионов. Между этими частями устанавливается динамическое равновесие. Часть свободного железа осаждается или поглощается живыми организмами. В то же время, часть закомплексованного железа распадается, восполняя концентрацию свободного железа и сохраняя равновесие. Т.е. происходит медленное, но непрерывное осаждение или поглощение свободного железа и, соответственно, уменьшение концентрации закомплексованного железа.
Цитата:
Сообщение от Bactrian

Так там же органическая молекула EDDHSA, составляющая 94% комплекса - вот она при добавлении солянки и разрушается, ибо устойчива до рН=3. ИМХО.
|
При подкислении разрушается не EDDHSA, а Fe-EDDHSA, т.е. разрушается связь между Fe и EDDHSA (точнее говоря, равновесие смещается в сторону уменьшения концентрации исходного комплекса). При подщелачивании раствора происходит обратный процесс.
|

|

|
|
3 пользователей поблагодарили Володя Череп за данный пост:
|
|
 14.09.2008, 20:16
14.09.2008, 20:16
|
#72
|
|
Живу я тут
Регистрация: 31.01.2007
Адрес: Киев
Сообщений: 2,744
Поблагодарил(а) : 535
Поблагодарили 6,235 раз(а) в 1,351 сообщениях
|
Ответ: Відповідь: Ответ: Відповідь: Хелат железа. Химики, обьясните. ===www.aquaforum.ua===
Цитата:
Сообщение от Володя Череп

Залили солянкой - разрушили хелат, налили в аквариум - восстановили хелат.
Происходит то же, что и с ЭДТА - лиганд протонируется и исходный комплекс разрушается (точнее говоря, равновесие смещается в сторону уменьшения концентрации исходного комплекса). Приводит ли это к обесцвечиванию, или нет - не могу сказать.
При подкислении разрушается не EDDHSA, а Fe-EDDHSA, т.е. разрушается связь между Fe и EDDHSA (точнее говоря, равновесие смещается в сторону уменьшения концентрации исходного комплекса). При подщелачивании раствора происходит обратный процесс.
|
Если все вот так - залили солянку - комплекс Fe-EDDHSA диссоциировал на составляющие (при этом пропал жутко-интенсивный коричневый цвет), а при "выливании" в аквариум кислого раствора, допустим мы даже не изменили/сорвали рН в аквариуме, комплекс снова ассоциировал - все классно.
А что будет с жутким цветом?
По логике - он опять появится.... 
__________________
[URL="http://dramader.blogspot.com/"]Посетите мой блог[/URL]
|

|

|
 14.09.2008, 20:29
14.09.2008, 20:29
|
#73
|
|
Живу я тут
Регистрация: 28.06.2003
Адрес: Киев
Сообщений: 757
Поблагодарил(а) : 831
Поблагодарили 833 раз(а) в 397 сообщениях
|
Відповідь: Хелат железа. Химики, обьясните. ===www.aquaforum.ua===
Смотря сколько залить. В любом случае, солянка на окрашивание воды в аквариуме влиять не должна: если дозировка небольшая, то и без солянки окрашивание будет незаметным, а если большая - то и с солянкой будет жуткий цвет.
|

|

|
 15.09.2008, 08:55
15.09.2008, 08:55
|
#74
|
|
Moderator
Регистрация: 28.02.2003
Адрес: Донецк
Сообщений: 5,562
Поблагодарил(а) : 1,630
Поблагодарили 3,504 раз(а) в 1,524 сообщениях
|
Ответ: Хелат железа. Химики, обьясните. ===www.aquaforum.ua===
Ребята, а вы сами пробовали обесцвечивать солянкой ?
Попробуйте, все вопросы отпадут сами собой.  __________________ 
|

|

|
 15.09.2008, 09:14
15.09.2008, 09:14
|
#75
|
|
Живу я тут
Регистрация: 31.01.2007
Адрес: Киев
Сообщений: 2,744
Поблагодарил(а) : 535
Поблагодарили 6,235 раз(а) в 1,351 сообщениях
|
Ответ: Хелат железа. Химики, обьясните. ===www.aquaforum.ua===
Цитата:
Сообщение от Vadim Art

Ребята, а вы сами пробовали обесцвечивать солянкой ?
Попробуйте, все вопросы отпадут сами собой.  |
А сколько надо солянки?
Каковы пропорции....
Я б с удовольствием попробовал...
Пропадает же кило железа...
Пробовал лимонной кислотой - не вышло... 
__________________
[URL="http://dramader.blogspot.com/"]Посетите мой блог[/URL]
|

|

|

 |
|
|
Здесь присутствуют: 1 (пользователей: 0 , гостей: 1)
|
|
|
 Ваши права в разделе
Ваши права в разделе
|
Вы не можете создавать новые темы
Вы не можете отвечать в темах
Вы не можете прикреплять вложения
Вы не можете редактировать свои сообщения
HTML код Выкл.
|
|
|
Текущее время: 16:31. Часовой пояс GMT +3.
|


