В аквариумной практике практике в качестве фосфорных удобрений используются калийные соли ортофосфорной кислоты. В большинстве случаев это оправдано. Однако в своей практике я встретился с таким несоответствием, при подаче рекомендуемых доз фосфора в соотношении N:P = 10:1, я получил рост ксенококуса, что указывает на недостаток фосфора. В одной из статей Ермолаева нашел, что он при борьбе с ксенококусом доводил соотношение до 1:0,5. В таком соотношении у меня наблюдалась только замедление роста ксенококуса.
Поэтому я решил по шерстить интернет. Вот, что я нашел.
На сайте
http://studopedia.ru/5_45335_proizve...vorimosti.html был найден ответ на количество фосфора в щелочной среде, при взаимодействии РО4 с Са получаем дигидрофосфат - Са3(РО4)2 который выподает в осадок. В этом случае фосфат-ионов в растворе будет находиться всего - 0,0118 мг/л, что явно недостаточно.
На следующем сайте нашел гидролиз фосфатов который идет в три этапа.
1) Гидролиз фосфатов выражается следующим уравнением:
К3PO4 + HOH ↔ K2HPO4 + KOH
При гидролизе образуется гидрофосфат-ион (HPO42-), который не диссоциирует на ионы. Среда определяется гидроксид-ионами (OH-). Среда раствора сильнощелочная.
2) Гидролиз гидрофосфатов протекает по следующему уравнению:
К2HPO4 + HOH ↔ KH2PO4 + KOH
Среда раствора дигидрофосфата является слабощелочной.
3) Гидролиз гидрофосфатов описывается уравнением:
KH2PO4 + HOH ↔ H3PO4 + KOH
среда раствора дигидрофосфата слабокислая.
Т.е. в результате гидролиза в растворе мы получаем гидроксид калия KOH и ортофосфорную кислоту H3PO4, а эти вещества, согласно орисанию к патенту Тарханова Олега Владимировича необходимы для состава по умягчению воды. Описание которого дано на
http://www.ntpo.com/patents_water/wa...ter_1282.shtml.
Однако данный процесс идет согласно данным сайта
http://www.abok.ru/for_spec/articles.php?nid=88 только в случае щелочной воды (pH 7,5 - 9,5). Для наглядности привожу данные взятые с этого сайта.
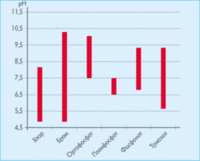
Выбор ингибиторов коррозии в зависимости от уровня pH воды.
Кроме этого в одной из диссертаций по водоочистке (к сожелению на сохранил адрес сайта) узнал, что на в Запорожье для смягчения вода применю фосфаты в колличестве до 85 мг/л.
Отсюда можно сделать вывод,что внося в щелочную воду фосфорные удобрения мы получаем умягчение воды, а не увеличение содержания фосфора в воде.
Для проверки этого вывода сделал такой опыт.
В стакан набрал 200г воды с общей жесткостью 18* и карбонатной - 12*, добавил 200 мг KH2PO4.
На следующий день получил такой результат общая жесткость 16* и карбонатная - 13*
через день общая жесткость 6* и карбонатной - 3*.
Превышение вносимой KH2PO4 взято для ускорения реакции между фосфором и кальцием.
P.S. В кислой и нейтральной воде дигидрофосфат - Са3(РО4)2 не образуется и мы получает только гидрофосфат CaHPO4 который хорошо растворяется в воде и не влияет на количество вносимого удо.


