 |
|
 03.09.2008, 21:52
03.09.2008, 21:52
|
#1
|
|
Живу я тут
Регистрация: 09.10.2005
Адрес: Киев
Сообщений: 10,140
Поблагодарил(а) : 11,373
Поблагодарили 9,058 раз(а) в 4,069 сообщениях
|
Відповідь: Хелат железа. Химики, обьясните. ===www.aquaforum.ua===
Цитата:
|
Сообщение от Кокан
А какая валентности этого самого (Edta) в соединении Fe(Edta), на пример?
|
А как понятие валентности соотносится с комплексообразованием? ИМНо это совсем разные консерватории.
И ЭДТА в количестве 1н штук может удержать сама железо (равно как магний, марганец и пр).
Другое дело, что я не очень понимаю принцип кормежки таким комплексом. ЭДТА в биохимии добавляют обычно для того, чтобы связать металлы и таким образом заблокировать ферментативные реакции. То есть комплекс должен распастся, чтобы железо дошло по назвачению? А что ему помешает окислиться при этом? Если ничто, то может лить купорос (сунуть гвозди) и не придумывать себе проблем?
|

|

|
 03.09.2008, 23:24
03.09.2008, 23:24
|
#2
|
|
Живу я тут
Регистрация: 28.06.2003
Адрес: Киев
Сообщений: 757
Поблагодарил(а) : 831
Поблагодарили 833 раз(а) в 397 сообщениях
|
Відповідь: Хелат железа. Химики, обьясните. ===www.aquaforum.ua===
Именно так. При такой большой концентрации кислорода, как в аквариумной воде, и такой небольшой концентрации восстановителя, как допускается из соображений нетоксичности, окислиться железу не помешает ничто.
В сельскохозяйственной литературе пишут, что хелатированное железо лучше усваивается растениями, чем нехелатированное, причем, для разных хелатов усваивается по-разному. Поэтому железо хелатируют, а о степени окисления не заботятся.
Но есть у аквариумистов надежда, подкрепленная рассуждениями и наблюдениями энтузиастов, что комплексы с Fe(2+) лучше усваиваются растениями, чем комплексы с Fe(3+), и не способствуют росту водорослей. Вот мы ради этой надежды и стараемся.
Добавлено через 1 час 33 минуты
Цитата:
Сообщение от red1157

Суть вопроса - на третий день в бутылке наблюдаю обильный белыйкристалический осадок, что это?
|
На форуме химиков недавно поднимался подобный вопрос. Говорят, что это белый протонированный комплекс Fe(2+) (т.е. FeH2(Edta)):
http://www.chemport.ru/guest2/viewtopic.php?f=4&t=22842&start=19
Ссылка на начало темы:
http://www.chemport.ru/guest2/viewtopic.php?f=4&t=22842&start=0
Последний раз редактировалось Володя Череп; 04.09.2008 в 00:57..
Причина: Добавлено сообщение
|

|

|
|
5 пользователей поблагодарили Володя Череп за данный пост:
|
|
 14.09.2008, 00:47
14.09.2008, 00:47
|
#3
|
|
Живу я тут
Регистрация: 09.10.2005
Адрес: Киев
Сообщений: 10,140
Поблагодарил(а) : 11,373
Поблагодарили 9,058 раз(а) в 4,069 сообщениях
|
Відповідь: Хелат железа. Химики, обьясните. ===www.aquaforum.ua===
Добавление кислоты не повышает, а понижает рН  А вот почему подкисление приводит к обесцвечиванию и не разрушается ли комплекс - не знаю. Может Володя Череп подскажет. А вообще все это алхимия. Если железо в комплексе - оно явно реакционно не доступно. Как распадается комплекс в аквариуме (линейно, логарифмически, моментально) - никто особо не мерял. Как быстро 2+ переходит в 3+ - тоже.
Последний раз редактировалось Mykhaylo; 14.09.2008 в 00:58..
|

|

|
 14.09.2008, 01:32
14.09.2008, 01:32
|
#4
|
|
Любитель отечественной флоры и фауны
Регистрация: 03.11.2003
Адрес: Киев
Сообщений: 5,563
Поблагодарил(а) : 4,179
Поблагодарили 3,075 раз(а) в 1,438 сообщениях
|
Ответ: Відповідь: Хелат железа. Химики, обьясните. ===www.aquaforum.ua===
Mykhaylo, Ты с кем сейчас разговаривал?
Добавлено через 18 минут
Главное ьлить в аквариум залезо шоб зелёное было. Это показатель 2+ . все , что не красное, то 2+. А вот если - 3+ на вас нападут водоросли, которые не попустят вас до конца..... А 3+ это красное. Бойтесь красного. ПРИМУ БЕЗ ФИЛЬТРА КУРИТЬ - ЗАПАДЛО!!!!!!
__________________
Ψ http://florastim.com.ua/
Последний раз редактировалось Кокан; 14.09.2008 в 01:51..
Причина: Добавлено сообщение
|

|

|
 14.09.2008, 11:23
14.09.2008, 11:23
|
#5
|
|
Живу я тут
Регистрация: 31.01.2007
Адрес: Киев
Сообщений: 2,744
Поблагодарил(а) : 535
Поблагодарили 6,235 раз(а) в 1,351 сообщениях
|
Ответ: Відповідь: Хелат железа. Химики, обьясните. ===www.aquaforum.ua===
Цитата:
Сообщение от Mykhaylo

Если железо в комплексе - оно явно реакционно не доступно. Как распадается комплекс в аквариуме (линейно, логарифмически, моментально) - никто особо не мерял. Как быстро 2+ переходит в 3+ - тоже.
|
Так там же органическая молекула EDDHSA, составляющая 94% комплекса
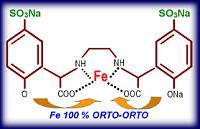
- вот она при добавлении солянки и разрушается, ибо устойчива до рН=3. ИМХО.
И остается катион железа, который по быстренькому, находит с чем связаться в растворе... и связывается ... или не находит... и тогда плавает как г...но в ополонке, но и его при этом ничто не защищает.
И вот такую "бурду" лить в аквариум?
Наверное это правильно, я ж не спорю...
Только мне как-то больше цитрат железа греет душу. 
Просто, дешево и эффективно...
__________________
[URL="http://dramader.blogspot.com/"]Посетите мой блог[/URL]
|

|

|
| Реклама помогает развиваться |
|
|
 14.09.2008, 20:05
14.09.2008, 20:05
|
#6
|
|
Живу я тут
Регистрация: 28.06.2003
Адрес: Киев
Сообщений: 757
Поблагодарил(а) : 831
Поблагодарили 833 раз(а) в 397 сообщениях
|
Відповідь: Ответ: Відповідь: Хелат железа. Химики, обьясните. ===www.aquaforum.ua===
Цитата:
Сообщение от Bactrian

Чего-то я не понимаю логики - взять хелат железа ... залить его солянкой - типа разрушить хелат - и что мы в результате в аквариум льём? Нехелатированное железо?
|
Залили солянкой - разрушили хелат, налили в аквариум - восстановили хелат.
Цитата:
Сообщение от Mykhaylo

А вот почему подкисление приводит к обесцвечиванию и не разрушается ли комплекс - не знаю. Может Володя Череп подскажет.
|
Происходит то же, что и с ЭДТА - лиганд протонируется и исходный комплекс разрушается (точнее говоря, равновесие смещается в сторону уменьшения концентрации исходного комплекса). Приводит ли это к обесцвечиванию, или нет - не могу сказать.
Цитата:
Сообщение от Mykhaylo

Если железо в комплексе - оно явно реакционно не доступно.
|
В комплексе находится большая часть железа. Меньшая часть железа находится в виде свободных катионов. Между этими частями устанавливается динамическое равновесие. Часть свободного железа осаждается или поглощается живыми организмами. В то же время, часть закомплексованного железа распадается, восполняя концентрацию свободного железа и сохраняя равновесие. Т.е. происходит медленное, но непрерывное осаждение или поглощение свободного железа и, соответственно, уменьшение концентрации закомплексованного железа.
Цитата:
Сообщение от Bactrian

Так там же органическая молекула EDDHSA, составляющая 94% комплекса - вот она при добавлении солянки и разрушается, ибо устойчива до рН=3. ИМХО.
|
При подкислении разрушается не EDDHSA, а Fe-EDDHSA, т.е. разрушается связь между Fe и EDDHSA (точнее говоря, равновесие смещается в сторону уменьшения концентрации исходного комплекса). При подщелачивании раствора происходит обратный процесс.
|

|

|
|
3 пользователей поблагодарили Володя Череп за данный пост:
|
|
 14.09.2008, 20:16
14.09.2008, 20:16
|
#7
|
|
Живу я тут
Регистрация: 31.01.2007
Адрес: Киев
Сообщений: 2,744
Поблагодарил(а) : 535
Поблагодарили 6,235 раз(а) в 1,351 сообщениях
|
Ответ: Відповідь: Ответ: Відповідь: Хелат железа. Химики, обьясните. ===www.aquaforum.ua===
Цитата:
Сообщение от Володя Череп

Залили солянкой - разрушили хелат, налили в аквариум - восстановили хелат.
Происходит то же, что и с ЭДТА - лиганд протонируется и исходный комплекс разрушается (точнее говоря, равновесие смещается в сторону уменьшения концентрации исходного комплекса). Приводит ли это к обесцвечиванию, или нет - не могу сказать.
При подкислении разрушается не EDDHSA, а Fe-EDDHSA, т.е. разрушается связь между Fe и EDDHSA (точнее говоря, равновесие смещается в сторону уменьшения концентрации исходного комплекса). При подщелачивании раствора происходит обратный процесс.
|
Если все вот так - залили солянку - комплекс Fe-EDDHSA диссоциировал на составляющие (при этом пропал жутко-интенсивный коричневый цвет), а при "выливании" в аквариум кислого раствора, допустим мы даже не изменили/сорвали рН в аквариуме, комплекс снова ассоциировал - все классно.
А что будет с жутким цветом?
По логике - он опять появится.... 
__________________
[URL="http://dramader.blogspot.com/"]Посетите мой блог[/URL]
|

|

|
 14.09.2008, 11:24
14.09.2008, 11:24
|
#8
|
|
Живу я тут
Регистрация: 09.10.2005
Адрес: Киев
Сообщений: 10,140
Поблагодарил(а) : 11,373
Поблагодарили 9,058 раз(а) в 4,069 сообщениях
|
Відповідь: Хелат железа. Химики, обьясните. ===www.aquaforum.ua===
2 Кокан
Зеленое и желтое железо - это для сульфата без комплексона.
В составе комплекса с ЭДТА железо что 2+, что 3+ - желтое. 
А курить вообще вредно, неважно что. 
2 Bactrian
Я не настаиваю что обесцвечивать кислотой - правильно, я не знаю что при этом происходит. Может туда краситель добавляют для пущего эффекта, как в тотему тутти-фрутти.
Судя по графикам до рН 3 не разрушается. Как по мне, то если хочется железа 2+, но нужно делать капельную подачу (или хотя бы ежедневное внесение) и не заморачиваться с устойчивостью комплекса и т.п.
|

|

|
 14.09.2008, 12:01
14.09.2008, 12:01
|
#9
|
|
Живу я тут
Регистрация: 31.01.2007
Адрес: Киев
Сообщений: 2,744
Поблагодарил(а) : 535
Поблагодарили 6,235 раз(а) в 1,351 сообщениях
|
Ответ: Відповідь: Хелат железа. Химики, обьясните. ===www.aquaforum.ua===
Цитата:
Сообщение от Mykhaylo

Я не настаиваю что обесцвечивать кислотой - правильно, я не знаю что при этом происходит. Может туда краситель добавляют для пущего эффекта, как в тотему тутти-фрутти.
Судя по графикам до рН 3 не разрушается. Как по мне, то если хочется железа 2+, но нужно делать капельную подачу (или хотя бы ежедневное внесение) и не заморачиваться с устойчивостью комплекса и т.п.
|
Куплю кислоты попробую... что там происходит.
Но, вот с чем согласен полностью - так это с частым внесением железа в аквариум... я вношу через день.
__________________
[URL="http://dramader.blogspot.com/"]Посетите мой блог[/URL]
|

|

|
 14.09.2008, 20:29
14.09.2008, 20:29
|
#10
|
|
Живу я тут
Регистрация: 28.06.2003
Адрес: Киев
Сообщений: 757
Поблагодарил(а) : 831
Поблагодарили 833 раз(а) в 397 сообщениях
|
Відповідь: Хелат железа. Химики, обьясните. ===www.aquaforum.ua===
Смотря сколько залить. В любом случае, солянка на окрашивание воды в аквариуме влиять не должна: если дозировка небольшая, то и без солянки окрашивание будет незаметным, а если большая - то и с солянкой будет жуткий цвет.
|

|

|
 15.09.2008, 08:55
15.09.2008, 08:55
|
#11
|
|
Moderator
Регистрация: 28.02.2003
Адрес: Донецк
Сообщений: 5,562
Поблагодарил(а) : 1,630
Поблагодарили 3,504 раз(а) в 1,524 сообщениях
|
Ответ: Хелат железа. Химики, обьясните. ===www.aquaforum.ua===
Ребята, а вы сами пробовали обесцвечивать солянкой ?
Попробуйте, все вопросы отпадут сами собой.  __________________ 
|

|

|
 15.09.2008, 09:14
15.09.2008, 09:14
|
#12
|
|
Живу я тут
Регистрация: 31.01.2007
Адрес: Киев
Сообщений: 2,744
Поблагодарил(а) : 535
Поблагодарили 6,235 раз(а) в 1,351 сообщениях
|
Ответ: Хелат железа. Химики, обьясните. ===www.aquaforum.ua===
Цитата:
Сообщение от Vadim Art

Ребята, а вы сами пробовали обесцвечивать солянкой ?
Попробуйте, все вопросы отпадут сами собой.  |
А сколько надо солянки?
Каковы пропорции....
Я б с удовольствием попробовал...
Пропадает же кило железа...
Пробовал лимонной кислотой - не вышло... 
__________________
[URL="http://dramader.blogspot.com/"]Посетите мой блог[/URL]
|

|

|
 15.09.2008, 10:45
15.09.2008, 10:45
|
#13
|
|
Живу я тут
Регистрация: 28.06.2003
Адрес: Киев
Сообщений: 757
Поблагодарил(а) : 831
Поблагодарили 833 раз(а) в 397 сообщениях
|
Відповідь: Хелат железа. Химики, обьясните. ===www.aquaforum.ua===
Солянку надо добавлять до исчезновения окраски или исчезновения солянки. 
|

|

|
 15.09.2008, 18:13
15.09.2008, 18:13
|
#14
|
|
Moderator
Регистрация: 28.02.2003
Адрес: Донецк
Сообщений: 5,562
Поблагодарил(а) : 1,630
Поблагодарили 3,504 раз(а) в 1,524 сообщениях
|
Ответ: Хелат железа. Химики, обьясните. ===www.aquaforum.ua===
солянки надо много. Пропорций уже не помню, но затею забросил.
Думаю, что пошутил Рома.
__________________ 
|

|

|
 15.09.2008, 18:26
15.09.2008, 18:26
|
#15
|
|
Живу я тут
Регистрация: 15.03.2007
Адрес: Г. Одесса.Таирово
Сообщений: 103
Поблагодарил(а) : 59
Поблагодарили 18 раз(а) в 17 сообщениях
|
Ответ: Хелат железа. Химики, обьясните. ===www.aquaforum.ua===
Ребята я не химик,но у меня есть из нета стотейка правда без сылки на первоисточник.Можно сюда кинуть? Может поможет.Там в статье есть еще пару сылок по этой теме.
Добавлено через 13 минут
Вот этот топик,но первоисточника нет,скачивал для себя.Модераторы удолите если не поправилам форума.
А чего бы самостоятельно не попытатся приготовить удобрения?
При всем уважении, у вас речь идет про "форсированные" травники, а это уже совсем другой подход.
Это не Флорена, Плантамин и Ферропол.
Это МАКРО и МИКРО...
Есть подход европейцев, есть система американцев, японцев...
Вот перевод, уже упоминавшейся в этом треде статьи:
http://aquahouse.com.ua/e107_plugins...php?content.15
Я тоже "упражнялся" в http://aquahouse.com.ua/e107_plugins...wtopic.php?792 - это для ленивых.
На http://amania.110mb.com/Chapters/Tech/diy-main.html расписано все достаточно подробно и по самоприготовлению, и по базовым системам - это, для само-определения.
Мне больше нравится подход американцев - это на сайте Тома Бара - его Estimated Index
наиболее подходит для хорошо разогнаных банок с "пустым" грунтом.
Я использую вот такой http://www.cherniaksoftware.com/home.../NutriCalc.exe, его рекомендуют
http://www.barrreport.com/estimative...test-kits.html
По этому калькулятору посчитал растворы солей
Надо получить такие вот концентрации
20 ppm KNO3 (ppm - одна часть на миллион)
30 ppm K2So4
3.0 ppm KH2Po4
10-50 ppm MgSo4 или больше (в качествеі Gh бустера для коррекцыи осмоса)
Для 100 литров Аквариума надо такие количества:
1.34 гр KNO3
0.63 гр K2SO4
0.39 гр KH2PO4
3.58 гр MgSO4
А вот такие растворы делать надо:
41.4 гр KNO3 растворить в 300 мл воды.
18.9 гр K2SO4 растворить в 300 мл воды.
11.7 гр KH2PO4 растворить в 300 мл воды.
107.4 гр MgSO4растворить в 300 мл воды.
Теперь каждого раствора можно брать по 1 мл на 10 литров воды аквариума и добавлять три раза в неделю.
По остальным дням надо добавлять МИКРО ( TMG або CSM+B по этому рецепту надо на аманию сходить http://amania.110mb.com/Chapters/Tech/liqfert-main.html ) и железо - у вас тут много писали. А я сначала просто лил фирменный плантамин - и растениям было хорошо.
И не забывать в субботу заменить воду 50%.
Вот такие расчеты, а химию я учил давно... очень давно.
Если найдете ошибки - посмотрим, пересчитаем, может и поправим
Суть методики Estimated Index заключається в том, что ви добавляете заведомо большие, но еще не вредные дозы макроудобрений, чтобы они забили
поступление этих же веществ (нитратов и фосфатов) из рыбьего гов... отходов и держали соотношение фосфор - нитраты в аквариуме.
При таком подходе образуются излишки этих элементов в воде аквариума - вы их убираете при замене 50-70% воды... простой метод разбавления.
Грунт при таком методе нужен нейтральный, чтобы не сдвигать соотношение элементов.
Том утверждает, что вам не нужны будут тесты
И растения у него растут раскошные, НО
НАЧИНАТЬ ТАКОЙ "ФОРСАЖ" МОЖНО ТОЛЬКО В АКВАРИУМЕ, ГДЕ РАСТЕНИЯ УЖЕ РАСТУТ, И ХОРОШО РАСТУТ, И В БОЛЬШОМ КОЛИЧЕСТВT Co2 подается не меньше 30 мг/л и свет выставлен не меньше вата на литр.
Если растений мало - вы получите водоросли в огромных количествах
Последний раз редактировалось Митя; 15.09.2008 в 18:40..
Причина: Добавлено сообщение
|

|

|
|
Пользователь, который поблагодарил Митя за данный пост:
|
|

 |
|
|
Здесь присутствуют: 1 (пользователей: 0 , гостей: 1)
|
|
|
 Ваши права в разделе
Ваши права в разделе
|
Вы не можете создавать новые темы
Вы не можете отвечать в темах
Вы не можете прикреплять вложения
Вы не можете редактировать свои сообщения
HTML код Выкл.
|
|
|
Текущее время: 09:04. Часовой пояс GMT +3.
|


